Alors que la pandémie de COVID-19 se propageait, les scientifiques ont accéléré leurs efforts pour trouver un vaccin qui pourrait mettre fin aux verrouillages et à la distanciation sociale pour de bon. Cependant, l’émergence de la nouvelle mutation D614G du coronavirus 2 du syndrome respiratoire aigu sévère (SRAS-CoV-2) a soulevé de nombreuses questions, notamment si elle rendra le virus résistant aux vaccins produits contre les versions antérieures du virus. Une nouvelle étude publiée dans la revue Vaccins npj en octobre 2020 montre qu’il s’agit peut-être d’une crainte non fondée.

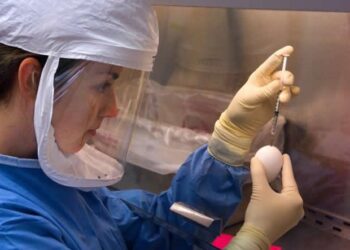
Cette image au microscope électronique à transmission montre le SARS-CoV-2, également connu sous le nom de 2019-nCoV, le virus qui cause le COVID-19. isolé d’un patient aux États-Unis, émergeant de la surface de cellules cultivées en laboratoire Image capturée et colorisée au NIAID’s Rocky Mountain Laboratories (RML) à Hamilton, Montana. Crédit: NIAID
Sommaire
Pourquoi la mutation D614G est-elle importante?
La plupart des vaccins candidats ciblent la protéine de pointe (S), qui existe sous la forme d’un homotrimère à la surface de l’enveloppe du virus. La glycoprotéine de pointe est le facteur qui permet au virus de s’engager avec le récepteur de l’enzyme de conversion de l’angiotensine 2 (ACE2) sur la cellule hôte pour entrer et infecter la cellule.
Peu de temps après le début de la propagation de la pandémie, un seul changement de nucléotide A à G a été remarqué à la position 23403 dans le génome de référence de Wuhan-Hu-1, entraînant le remplacement d’un résidu d’aspartate par de la glycine à la position 614 de la protéine de pointe.
Depuis l’émergence de cette mutation, la variante DG614 est devenue dominante par rapport aux variantes antérieures, étant observée dans plus de 85% des séquences téléchargées du monde entier, jusqu’au 1er juillet 2020. Cela a conduit à l’hypothèse que les souches virales avec cette mutation présente un avantage structurel.
Peut-être, disent certains scientifiques, que de tels isolats se lient mieux au site de clivage de la furine sur la sous-unité S1. Cela permet au variant DG614 d’être plus transmissible, de se répliquer plus efficacement et de produire des charges virales plus élevées. En outre, les DG614 sont mieux adaptés pour entrer dans la cellule hôte humaine, sont plus pathogènes et peuvent être associés à une mortalité plus élevée.
Modélisation de l’efficacité des vaccins dans les souches D614G
L’étude actuelle dirigée par l’agence scientifique nationale australienne, le Commonwealth Scientific and Industrial Research Organization (CSIRO), a exploré l’impact possible de cette mutation sur l’efficacité des vaccins.
Les chercheurs ont utilisé du sérum de furets auquel le candidat vaccin COVID-19 a été conçu pour contrer la variante DG614 de la protéine S. Ces sérums ont été testés pour la capacité de neutralisation contre les isolats de SARS-CoV-2 avec et sans la mutation D614G, et par ailleurs comparables en ce qui concerne la liaison et l’entrée des cellules.
Les chercheurs ont utilisé les isolats australiens «VIC01» et «SA01» (qui sont D614) et «VIC31» (qui est DG614) dans les essais de neutralisation. Ils ont constaté que les furets avaient un titre médian d’anticorps neutralisants de 6,3 log contre les trois isolats. Dans l’ensemble, le titre moyen des anticorps neutralisants contre le variant G614 ressemblait à celui des variants D614.
Ils ont ensuite modélisé la protéine de pointe au niveau moléculaire pour découvrir la dynamique structurelle de la mutation, pour étudier l’effet possible de la mutation sur l’efficacité du vaccin et si la mutation conférait les avantages proposés par d’autres chercheurs.
Le site de mutation est en amont du site de clivage de la furine à l’interface S1 / S2 et est enterré sous la surface et protégé par une molécule de sucre à la position N616. Ainsi, ce n’est probablement pas un composant épitopique neutralisant et il est peu probable qu’il affecte l’efficacité neutralisante des anticorps générés par les vaccins à base de D614. Bien qu’il existe deux épitopes neutralisants à cet emplacement, la position S614 en est distincte.
La modélisation élimine l’avantage du site de clivage avec D614G
Des études antérieures montrent que la mutation D614G produit un site de clivage d’élastase. Pourtant, les simulations de dynamique moléculaire dans l’étude actuelle montrent que cela ne produit pas de clivage S1 / S2 médié par l’élastase, et n’affecte donc pas l’efficacité de réplication. Même si la furine peut accéder au site de clivage à l’interface, l’élastase ne peut pas sonder le site nouvellement introduit en raison de sa position enfouie et de son blindage, comme décrit ci-dessus, sans la séparation du capuchon trimère S1 et du S2.
Encore une fois, le site D614 sur S1 interagit avec S2 via des interactions de liaison hydrogène et un pont salin. La mutation G614 abolit le pont salin et, par conséquent, plutôt que d’améliorer l’interaction entre S1 et S2, elle peut réduire la stabilité.
Interactions supplémentaires
Les chercheurs ont simulé ces interactions dans l’orientation « vers le haut » du domaine de liaison au récepteur (RBD), mais ont également constaté que dans une courte simulation, l’ACE2 s’est incliné pour entrer en contact avec le RBD sur le monomère adjacent, par des contacts entre trois résidus. .
Cela indique la possibilité que le RBD adjacent dans la conformation «vers le bas» joue un rôle dans la liaison et la spécificité de l’ACE2. En fait, cela concorde avec des études antérieures montrant la nature flexible des interactions de protéines de pointe, où la protéine de pointe était capable de former un complexe avec ACE2 dans trois conformations différentes.
La mutation du site RdRp augmente l’infectivité
Une autre découverte pertinente est que la mutation D614G est également associée à une mutation C-à-U en position 14 408, provoquant une mutation Pro-Leu 314 dans orf1b qui code la polymérase ARN-dépendante (RdRp / nsp12). Cela peut être une raison de l’infectivité accrue de la nouvelle variante.
Cette mutation se situe dans une fente hydrophobe à proximité du site actif de l’enzyme. Cette fente est, selon le modèle. doublé de résidus d’arginine et ceux-ci peuvent favoriser la liaison nucléotidique. Cela peut stabiliser la conformation localement, par ses effets sur les contraintes du squelette. Son impact sur la virulence est inconnu à l’heure actuelle, ce qui indique la nécessité de travailler davantage.
Implications
Les études futures doivent inclure des tests de protection des anticorps pour comprendre les effets de ces mutations sur les organismes vivants.
Dit l’auteur principal, le professeur Seshadri Vasan, « Malgré cette mutation D614G de la protéine de pointe, nous avons confirmé par des expériences et une modélisation que les candidats vaccins sont toujours efficaces«Ceci fournit aux efforts intensifs de développement de vaccins une justification claire pour procéder à l’achèvement.
Deuxièmement, dit-il, « Nous avons également constaté que la souche G ne nécessitera probablement pas de fréquents « appariements de vaccins » lorsque de nouveaux vaccins doivent être développés de manière saisonnière pour lutter contre les souches virales en circulation.. «
De plus, disent les chercheurs, étant donné la grande disponibilité des approches de modélisation, et pour assurer la confiance du public dans les vaccins une fois disponibles, « il serait souhaitable d’analyser l’impact des mutations identifiées, en collaboration avec ces organisations, avant de spéculer sur les effets indésirables potentiels sur les vaccins. »
A lire à ce sujet : 10 raisons de se faire vacciner contre le COVID-19