Dans un document révolutionnaire actuellement disponible sur le bioRxiv * serveur de préimpression, les chercheurs de la Washington University School of Medicine et de la Stony Brook University ont montré comment la protéine nucléocapside du syndrome respiratoire aigu sévère coronavirus 2 (SARS-CoV-2) est dynamique, désordonnée et se sépare en phases avec l'ARN – informant, à son tour, la découverte de médicaments qui perturbent l'emballage viral.

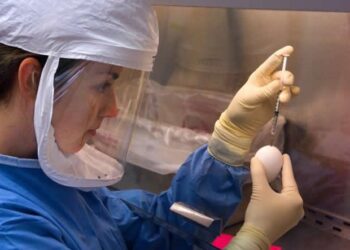
Novel Coronavirus SARS-CoV-2 Rendu créatif des particules du virus SARS-COV-2. Remarque: pas à l'échelle. Crédits: NIAID
La pandémie mondiale de coronavirus (COVID-19) s'accélère actuellement dans différentes parties du monde, tout comme les recherches sur les aspects fondamentaux de son agent causal, le virus nommé SARS-CoV-2. Néanmoins, nous n'avons toujours pas de médicament ou de vaccin approuvé, ce qui signifie que de nombreuses vies sont en jeu.
Ce que nous savons, c'est que la protéine nucléocapside SARS-CoV-2 est une protéine de liaison à l'ARN abondante qui joue de nombreux rôles dans le cycle de vie viral, tels que la réplication, la transcription et l'emballage du génome. Il partage de nombreuses caractéristiques de séquence avec d'autres protéines nucléocapsides de coronavirus.
Un corpus de travaux sur la protéine nucléocapside d'une pléthore de coronavirus modèles a révélé qu'elle subit une auto-association, une interaction spécifique avec d'autres protéines, ainsi qu'une interaction avec l'ARN acide nucléique – le tout de manière hautement multivalente.
Cependant, malgré sa nature décisive et multifonctionnelle, les détails moléculaires sur la façon dont la protéine nucléocapside intervient dans ces fonctions sont encore mal compris. Récemment, il a été signalé que la protéine nucléocapside subit une séparation de phases avec l'ARN.
Et comme il est connu que cette protéine est à la base de l'emballage viral, l'une des hypothèses est que la séparation de phases peut en fait représenter un épiphénomène inévitable qui reflète les propriétés physiques essentielles d'une protéine pour entraîner le compactage de longues molécules d'ARN.
C'est pourquoi un groupe de recherche de la Washington University School of Medicine et de la Stony Brook University a décidé de combiner la spectroscopie à molécule unique avec des simulations tous atomes pour dévoiler les détails moléculaires qui capturent la fonction de la protéine nucléocapside SARS-CoV-2.

Séquence et résumé structurel de la protéine N de l'architecture du domaine A de la protéine N du SRAS-CoV-2. Les positions des colorants utilisées dans cette étude sont annotées en haut, la prédiction des troubles calculée en bas. B Structure du domaine de liaison à l'ARN du SARS-CoV-2 (RBD) (PBD: 6yi3). Centre et gauche: coloré en fonction du potentiel de surface, révélant la surface très basique du RBD. À droite: structure en ruban avec les terminaisons N et C mises en évidence.
Sommaire
Constructions complètes de la protéine nucléocapside
Le but de cette approche était en fait de reconstruire une description atomistique de l'ensemble conformationnel de la protéine nucléocapside, ainsi que de cartographier ses interactions intrachaînes. À cette fin, ce groupe de recherche a créé trois constructions intégrales de la protéine nucléocapside avec des marqueurs fluorescents.
« Ces constructions nous ont permis de sonder les conformations et la dynamique des régions désordonnées dans le contexte de la protéine pleine longueur en utilisant le transfert d'énergie de résonance Förster (FRET) et la spectroscopie de corrélation de fluorescence (FCS) », expliquent les auteurs de l'étude.
Parallèlement à ces expériences, ils ont également effectué des simulations Monte Carlo tous atomes de chacune des trois régions intrinsèquement désordonnées isolément et en contexte avec leurs domaines repliés adjacents.
Démêler le lien complexe des interactions
Cette étude a révélé que la protéine nucléocapside subit fermement la séparation de phases in vitro avec l'ARN modèle dans une gamme de différentes conditions de sel. En utilisant des modèles de polymère simples, les chercheurs ont en outre révélé que les mêmes interactions qui conduisent à la séparation de phase pourraient également conduire le conditionnement du génome dans un condensat dynamique à un seul génome.
Plus précisément, ce modèle a suggéré que la symétrie traversant un petit nombre de sites de liaison de haute affinité peut en effet organiser des interactions multivalentes anisotropes pour conduire au compactage monopolymère, assez différent de la séparation de phases multipolymère.
« Nous proposons un modèle simple dans lequel la symétrie traversant des sites de liaison spécifiques favorise la formation de condensats métastables à ARN unique, par opposition aux grosses gouttelettes multi-ARN à phases séparées », ont déclaré les auteurs de l'étude.
Et comme observé pour d'autres protéines ayant des caractéristiques moléculaires similaires, les chercheurs ont découvert que la protéine nucléocapside subit une séparation de phase liquide-liquide lorsqu'elle est mélangée à de l'ARN. De plus, les modèles de polymères prévoient que les mêmes interactions multivalentes qui entraînent la séparation de phases engendrent également le compactage de l'ARN.
« Indépendamment de son rôle physiologique, nos résultats suggèrent que la séparation de phases fournit une lecture macroscopique (gouttelettes visibles) d'un processus nanoscopique (protéine: ARN et protéine: protéine interaction) », expliquent davantage les auteurs de l'étude.

A. Résumé des résultats des expériences de spectroscopie à molécule unique et des simulations de tous les atomes. Les trois IDR prédits sont désordonnés, très flexibles et abritent un certain nombre de régions de liaison hélicoïdale putatives qui se chevauchent avec les sous-régions identifiées précédemment pour piloter la fonction des protéines N. B. Aperçu du modèle général de rupture de symétrie. Pour les polymères homopolymères, l'effondrement local conduit à des condensats monopolymères qui subissent une fusion sans barrière, s'assemblant rapidement en grands condensats multipolymères. Lorsqu'un (ou un petit nombre de) sites à affinité élevée sont présents, un regroupement local de liants à une concentration plus faible organise le polymère de telle sorte que les condensats de polymère unique sont cinétiquement stables. C. Modèle proposé pour l'emballage du génome du SRAS-CoV-2. (1) Un modèle simplifié du génome du SRAS-CoV-2 avec une paire de régions de conditionnement aux extrémités 5 'et 3' du génome (2) La protéine N se lie de préférence aux régions de signaux de conditionnement dans le génome, conduisant à un cluster local de la protéine N à l'ARN du signal de conditionnement. (3) La concentration locale élevée de protéine N entraîne la condensation des régions distales du génome, formant un condensat stable d'un seul génome. (4) Les condensats d'un seul génome peuvent subir une maturation ultérieure par une transition liquide-solide (cristallisation) pour former une capside cristalline ordonnée ou se solidifier en une particule ribonucléaire amorphe (RNP). Alors que dans certains virus, une capside ordonnée se forme clairement, nous privilégions un modèle dans lequel la capside SARS-CoV-2 est une RNP amorphe. Le condensat compact d'un seul génome recrute finalement des protéines E, S et M à la membrane, entraînant la formation de l'enveloppe et le conditionnement final des virions.
Médicaments qui perturbent l'emballage viral
Selon leurs résultats, les chercheurs postulent que le conditionnement viral peut impliquer un compactage initial du génome via des interactions protéine multivalente: ARN et protéine: protéine, qui est ensuite suivie d'une transition liquide-solide dans les cas où des structures de capside cristalline bien définies émergent.
« Nous supposons que le compactage de l'ARN pour former des condensats dynamiques d'un seul génome peut être à l'origine des premiers stades de l'emballage du génome », affirment les auteurs de l'étude. « En tant que tels, des tests qui mesurent comment les composés modulent la séparation de phases pourraient fournir un outil pratique pour identifier les médicaments qui perturbent l'emballage viral », ajoutent-ils.
Le modèle est également en accord empirique suffisant avec les observations récentes faites pour d'autres agents viraux, suggérant à son tour que la nature s'appuie sur les mêmes principes qu'un mécanisme évolué pour l'assemblage de particules monodisperses.
En conclusion, il y a des implications thérapeutiques significatives de la compréhension et de la modulation de la séparation de phases ici (mais aussi ailleurs en biologie), et ces résultats offrent une fenêtre sur les interactions physiques critiques.
*Avis important
bioRxiv publie des rapports scientifiques préliminaires qui ne sont pas évalués par des pairs et, par conséquent, ne doivent pas être considérés comme concluants, orienter la pratique clinique / les comportements liés à la santé, ou traités comme des informations établies.