Une nouvelle étude menée par des chercheurs du Centre de recherche allemand de Jülich rapporte l'inhibition de l'agrégation et de l'activation de la protéine de récepteur de pointe du virus provoquant la pandémie actuelle, par un peptide sur le récepteur de l'enzyme de conversion de l'angiotensine 2 (ACE2). La recherche est publiée sur le serveur de préimpression bioRxiv * en juin 2020 et soumis à la Journal biophysique pour examen par les pairs.
La pandémie en cours a commencé à Wuhan en Chine, avec un groupe d'infections causées par un nouveau coronavirus. Cela a été identifié plus tard et nommé SARS-CoV-2 (syndrome respiratoire aigu sévère coronavirus 2), et le syndrome a été appelé coronavirus 2019 (COVID-19). La maladie s'est rapidement propagée dans le monde entier, l'épicentre se déplaçant de la Chine vers l'Asie du Sud-Est, puis vers l'Europe, et enfin vers les États-Unis.

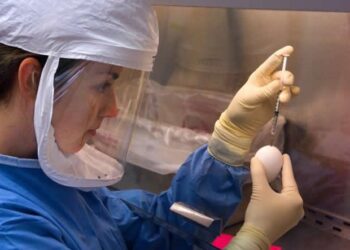
NIAIDSuivez le nouveau coronavirus SARS-CoV-2 Micrographie électronique à balayage colorisée d'une cellule VERO E6 (bronzage) présentant des projections cellulaires allongées et des signes d'apoptose, après infection par des particules de virus SARS-COV-2 (vertes), qui ont été isolées d'un échantillon de patient . Image capturée au NIAID Integrated Research Facility (IRF) à Fort Detrick, Maryland. Crédits: NIAID
Pendant ce temps, les épidémies en Inde, en Russie et au Brésil se poursuivent pour la plupart sans contrôle, le nombre de décès dans le monde dépassant maintenant 400 000 et le nombre de cas approchant les 7 millions et augmentant. L'impact de la pandémie a été ressenti par un lourd tribut sur la vie et la santé humaines, ainsi que par les perturbations économiques dans presque tous les pays du monde.
Il n'est donc pas surprenant que les scientifiques se précipitent pour trouver un vaccin ou un médicament antiviral. L'une de ces cibles vaccinales est la protéine spike (S) du coronavirus, car elle facilite l'entrée virale dans la cellule. La protéine S est présente sous forme de trimères, avec deux sous-unités, S1 et S2, comprenant chaque trimère.

(a) Structure cristalline du domaine du récepteur de la pointe du CoV-2 du SRAS liée à l'ACE2 (PDB: 6M0J (19)). ACE2 montré en bleu, cyan, jaune et vert, le domaine du récepteur Spike est montré en orange. (b) 20 différentes conformations d'hexapeptide (YKYRYL) utilisées comme modèles de départ initiaux de simulations MD d'équilibre indépendant de 50 ns dans un solvant explicite. (c) Structure de départ de la simulation d'agrégation améliorée du domaine du récepteur de pointe à ACE2. (d) Structure de départ de la simulation d'agrégation améliorée du même agrégat en présence de l'hexapeptide.
Sommaire
Comment se déroule l'entrée virale?
La sous-unité S1 de la protéine S est impliquée dans la fixation du virus à la surface cellulaire, tandis que la sous-unité S2 participe à la fusion membranaire. Ainsi, le virus nécessite la molécule ACE2 à la surface cellulaire comme récepteur d'entrée, pour permettre la fusion membranaire. En même temps, l'hôte TMPRSS2, une sérine protéase transmembranaire, est impliquée dans l'amorçage de la protéine S avant que cela ne puisse se produire.
Le SRAS-CoV-2 peut faire le saut entre les espèces pour infecter facilement les humains car le récepteur ACE2 est hautement conservé entre les différentes espèces de mammifères. La sous-unité S2 de la protéine S possède un domaine de liaison au récepteur (RBD) qui correspond à la molécule ACE2.
Le RBD a 5 hélices bêta fonctionnant en antiparallèle, tandis que des motifs alpha-hélicoïdaux et en boucle relient les feuilles bêta. Le motif de liaison au récepteur (RBM) est une insertion prolongée entre une paire de feuilles bêta, et cela se lie à l'extrémité N-terminale de la molécule ACE2.
Un mécanisme efficace pour prévenir l'infection virale et contenir ainsi l'épidémie pourrait être l'inhibition de l'interaction de la protéine ACE2-S qui mène à l'entrée virale. Dans la présente étude, un hexapeptide ((438) YKYRYL (443)) qui appartient au domaine récepteur du virus s'est révélé inhiber efficacement cette interaction.
L'hexapeptide inhibiteur
Des expériences in vitro ont montré que ce peptide empêchait l'infection des cultures cellulaires par le SARS-CoV antérieur. De plus, il a été constaté que ce peptide empêche également un autre coronavirus, CoV-NL63, de se répliquer. Fait intéressant, ce fragment de protéine a une affinité élevée pour ACE2, étant l'emplacement de l'épitope de liaison dominant. Son mode de fixation est bien établi par diverses techniques d'imagerie, de sorte qu'il a le potentiel d'être utilisé comme modèle pour les inhibiteurs d'entrée contre le SRAS-CoV et les virus similaires.
Les chercheurs ont étudié plus en détail l'interaction ACE2-peptide en utilisant une technique appelée dynamique moléculaire (MD) pour fournir des simulations puissantes. Il s'agit donc d'un outil in silico utile qui ajoute aux connaissances fournies par les études expérimentales.
Découvrir les mécanismes de liaison de l'hexapeptide
Les objectifs de l'étude étaient, tout d'abord, de quantifier l'affinité de liaison de la protéine S à la molécule ACE2. Deuxièmement, les chercheurs ont utilisé la DM pour évaluer l'énergie libre libérée lorsque le ligand s'adsorbe sur son site de liaison au niveau du récepteur ACE2. Troisièmement, ils ont examiné comment le peptide affecte l'interaction protéine S-ACE2.
L'étude montre que l'hexapeptide a une affinité de liaison élevée avec le récepteur au niveau de 3 grappes dans la région N-terminale. Selon des études aux rayons X, ces grappes sont situées à l'interface de la protéine de pointe et du récepteur. Avec la liaison à l'hexapeptide, la protéine réceptrice de pointe s'est détendue en un minimum d'énergie qui était assez différent de la structure des rayons X.
La protéine S tourne maintenant à cause de la répulsion électrostatique, après quoi elle se lie à la molécule ACE2 à un patch hydrophobe plutôt que via le RBM comme suggéré par les expériences. Cela est dû au minimum d'énergie.
Les simulations montrent que lorsque l'hexapeptide est présent, il se lie à la protéine S près du site de liaison à la molécule ACE2. Suite à cette liaison, la protéine S modifie son schéma d'agrégation vers le récepteur.
L'hexapeptide se lie d'abord à la protéine réceptrice de pointe, avec un contact secondaire à un autre endroit. L'hexapeptide diffuse ensuite le long de la surface du domaine du récepteur de pointe jusqu'à ce qu'il se lie finalement fortement à la protéine de pointe. Le RBM tourne loin de la surface de l'ACE2 en raison des interactions électrostatiques, mais la liaison du RBD à l'hélice N-terminale, 4 nm plus loin de la conformation qui se produit lorsque l'hexapeptide n'est pas présent. Cette liaison très faible montre qu'elle est dans un état inhibé.
L'effet de l'hexapeptide
En d'autres termes, l'hexapeptide inhibe l'activation de l'ACE2 et empêche ainsi la fusion membranaire et l'entrée virale. Ainsi, la simulation et l'étude expérimentale montrent que cet hexapeptide pourrait être un nouveau mode de traitement pour empêcher l'entrée virale dans les cellules hôtes humaines. Si le peptide est clivé par des protéases, cela atténue l'effet inhibiteur de la première. Ainsi, pour augmenter son efficacité, le peptide pourrait avoir besoin d'être modifié chimiquement pour empêcher un tel clivage.
L'hexapeptide est également hautement spécifique de la protéine S et de la molécule ACE2. Comme cela exclut une autre fonction de ce peptide dans le corps humain, il peut être considéré pour le développement comme un médicament potentiel.
*Avis important
bioRxiv publie des rapports scientifiques préliminaires qui ne sont pas évalués par des pairs et, par conséquent, ne doivent pas être considérés comme concluants, orienter la pratique clinique / les comportements liés à la santé, ou traités comme des informations établies.