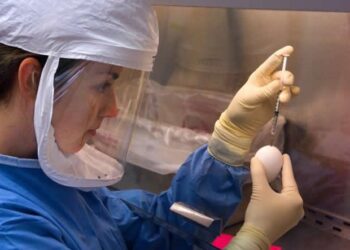
Les vaccins inactivés à cellules entières, également connus sous le nom de « vaccins tués », font partie des variétés de vaccins les plus traditionnellement utilisées, ayant été développés contre un large éventail d’agents pathogènes, y compris E. coli.
Dans une nouvelle étude, publiée sous forme de pré-impression sur le bioRxiv* serveur, une équipe de chercheurs inactivée cellule entière E. coli avec un génome réduit et l’a utilisé pour exprimer des peptides de fusion spécifiques du coronavirus, démontrant une réponse anamnestique puissante.

Conception du vaccin
Les bactéries à Gram négatif portent des protéines de transport, des autotransporteurs, qui permettent l’échange des protéines exprimées à la surface cellulaire, et le génie génétique moderne permet à une protéine d’intérêt de s’exprimer à la surface de cette manière. Jusqu’à 200 000 protéines étrangères peuvent être affichées à la surface d’une seule bactérie, et cette technologie a déjà été utilisée pour déclencher une réponse immunitaire. in vivo en affichant des antigènes pathogènes sélectionnés. Cependant, la gamme d’antigènes qui peuvent être exprimés par cette méthode est limitée par la taille, à moins d’environ 50 kDa, et les bactéries ne produisent pas de protéines avec une glycolysation mammifère, et peuvent donc ne pas provoquer la production des anticorps appropriés.
Aucun vaccin n’a encore été homologué qui emploie cette technologie, en grande partie en raison de la faible immunogénicité affichée en raison d’une glycolysation incorrecte. Dans cet article, le groupe a émis l’hypothèse que l’élimination des protéines de surface étrangères des bactéries, en plus de l’antigène d’intérêt exprimé, pourrait provoquer une réponse immunitaire plus forte. L’ensemble de la protéine de pointe du SRAS-CoV-2 utilisée dans les vaccins déployés est une grande protéine de 180 kDa et n’a donc pas pu être déployée en utilisant cette méthode. Plusieurs familles de virus, dont les coronavirus et le SRAS-CoV-2, portent le peptide de fusion VIH-1, qui est impliqué dans la pénétration de la membrane cellulaire. Comme cette région est hautement conservée, elle pourrait potentiellement constituer un bon candidat vaccin, et les auteurs soulignent en outre que l’utilisation de la protéine de pointe entière a été impliquée dans un risque accru de syndromes inflammatoires rares.
Tester le vaccin
Le groupe a utilisé des cellules entières tuées E. coli qui ont été génomiques réduits afin de présenter moins de protéines cellulaires de surface natives. Un plasmide a été inséré dans les bactéries pour exprimer le peptide de fusion VIH-1 spécifique du SARS-CoV-2, démontré par la suite par des tests de liaison d’anticorps. Des vaccins alternatifs ont également été préparés pour le virus de la diarrhée épidémique porcine (PEDV), exprimant le peptide de fusion corrélé pour ce virus similaire.
Les porcs ont été vaccinés avec l’un des vaccins préparés et un contrôle, administrés avec un rappel au jour 21, puis soumis à une infection orale à PEDV par le virus respectif au jour 35. Le sang a été prélevé chaque semaine et les anticorps anti-protéine de fusion circulants quantifiés, non étant significativement plus élevée après la vaccination mais avant le défi. Cependant, à la suite de la provocation virale, les valeurs anti-FP étaient notablement plus élevées parmi les vaccinés, suggérant que les vaccins avaient incité les porcs à répondre. Les taux sériques d’interféron-y étaient également plus élevés parmi les vaccinés, et moins de ces porcs ont exprimé des signes extérieurs de symptômes liés au PEDV.
Comme prévu, le vaccin PEDV s’est avéré plus efficace pour immuniser contre le PEDV que le vaccin SARS-CoV-2. Cependant, la similitude des protéines de fusion provenant de chaque virus était telle qu’une réponse statistiquement significative était toujours détectée. En effet, les 13 séquences d’acides aminés entourant les 6 résidus core de chaque séquence sont identiques.
Le groupe fait valoir que ces vaccins pourraient être plus faciles à produire et à transporter que les vaccins à ARNm actuellement déployés, en particulier compte tenu de la nécessité d’une chaîne du froid solide dans ce dernier cas, nécessitant des températures constantes de -20 ° C ou plus froides. Ils concèdent cependant que la possibilité de provoquer une réponse immunitaire chez les hôtes envers le génome réduit E. coli comporte un risque faible mais possible et nécessite une enquête plus approfondie.
*Avis important
bioRxiv publie des rapports scientifiques préliminaires qui ne sont pas évalués par des pairs et, par conséquent, ne doivent pas être considérés comme concluants, guider la pratique clinique / les comportements liés à la santé, ou traités comme des informations établies.